Actualités
Bientôt la fin de l’évaluation des risques pour les OGM ?

La gestion des OGM par l’Union européenne fait l’objet d’allègements incessants depuis 2013. Si cela concernait jusqu’à maintenant les OGM dits empilés car ayant plusieurs modifications génétiques (tolérance à plusieurs herbicides, tolérance herbicide + insecticide…), des discussions viennent d’être entamées entre États membres et Commission pour qu’un principe fondateur de la loi européenne sur les OGM tombe : la commercialisation d’OGM ayant une seule modification génétique pourrait être autorisée sans faire l’objet de demande dédiée au prétexte qu’une entreprise n’a pas l’intention de les commercialiser avec cette seule modification !
En 2018, Inf’OGM rapportait comment avaient été systématisées plusieurs simplifications de la procédure d’autorisation commerciale des OGM [1] [2] [3]. Cette dynamique, initiée en 2013, a abouti à un système très éloigné de l’approche voulue en 2001 par le législateur lors de l’adoption de la directive 2001/18, à savoir « une modification génétique revendiquée, une autorisation ». En 2021, ces simplifications continuent avec un énième allègement qui commence à se dessiner.
2013, année de légalisation des allègements
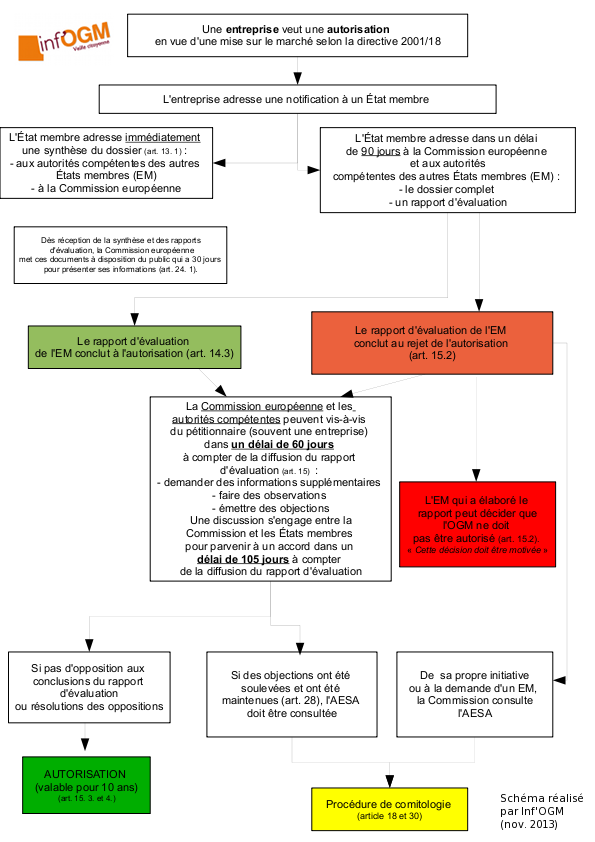
Lorsqu’il adopte la directive 2001/18 sur la dissémination des OGM dans l’environnement, le législateur européen reprend l’approche initiée en 1990 voulant que tout OGM soumis aux requis réglementaires doit faire l’objet d’une analyse préalable des risques potentiels avant d’être autorisé. Une approche connue sous l’expression « au cas par cas ». Qu’ils contiennent un seul événement de modification génétique (transgène, cisgène, séquence mutée…), qu’ils en contiennent deux, trois, huit… tous les OGM doivent être soumis à une évaluation des risques avec analyses d’alimentarité, de toxicologie, d’allergénicité…
Douze ans plus tard, l’adoption du règlement 503/2013 vient légaliser des pratiques institutionnelles qu’Inf’OGM qualifiait alors d’ »allégées« . Ainsi, pour un dossier de demande d’autorisation, il devenait légal de ne pas fournir toutes les données expérimentales requises par l’évaluation des risques dans les cas très généraux où des informations données ne sont pas nécessaires « compte tenu de la nature de la modification génétique ou du produit », « d’un point de vue scientifique » voire si « leur fourniture est techniquement impossible ».
Un autre allègement tout aussi conséquent avait lieu. L’approche « au cas par cas » était rompue par une simplification des procédures réduisant le nombre de demandes à déposer pour obtenir une autorisation commerciale. Dans le règlement 503/2013, le législateur constate que la mise en culture de semences d’une plante OGM empilée, à cinq modifications génétiques par exemple, conduit à l’apparition aux champs de plants OGM ayant les cinq modifications mais pouvant également en avoir quatre, trois, deux, une, voire zéro. Qualifiant la mise sur le marché de ces OGM comme « inévitable » [4], le législateur décidait que l’autorisation commerciale donnée pour l’OGM empilé vaudrait désormais autorisation pour les OGM ayant quatre, trois ou deux des cinq modifications. Une simplification substantielle puisque faisant passer de 26 à un le nombre de demande d’autorisation à déposer dans le cas d’un OGM empilé à cinq modifications génétiques. 26 OGM parmi lesquels 25 ne nécessitent plus de données expérimentales permettant leur analyse en termes de risque. En 2018, avec l’adoption de la directive 2018/350, cette simplification a été élargie à toutes les espèces de plantes et non plus restreinte aux seules plantes pouvant produire des sous-combinaisons aux champs (le cotonnier ne peut pas par exemple).
Cette approche posait question sur le seul plan de l’évaluation des risques. Car un même OGM à deux ou trois modifications génétiques peut être différent selon qu’il apparaît au champ ou qu’il est produit en laboratoire. Or, les deux sont couverts par la simplification administrative fournie par le règlement 503/2013. Si les experts européens de l’Autorité européenne de sécurité des aliments (AESA) eux-mêmes soulignaient ce point avant 2013 pour des raisons d’évaluation des risques, ils finirent par se ranger à la simplification administrative poussée par la Commission comme Inf’OGM l’avait montré [5]…
Une condition néanmoins limitait cette simplification : les OGM à une seule modification génétique devaient être soumis à une procédure d’évaluation des risques obligatoire et ne pouvaient être autorisés sous couvert d’une autorisation donnée à un OGM empilé. Mais ce principe fondateur est justement celui sur lequel les États membres se penchent depuis septembre 2020, avec l’aval de la Commission européenne !
Un nouveau cas particulier…
Le 15 septembre 2020, le Comité permanent sur les plantes, animaux, alimentation humaine et animale a un point singulier à son ordre du jour [6]. Dans le cadre d’une demande d’autorisation déposée pour le colza transgénique Ms11*Rf3, la Commission européenne explique aux représentants des États membres que « le pétitionnaire a confirmé que le colza Ms11 n’est pas destiné à la commercialisation en tant que tel (mais est destiné à être utilisé dans un empilement) ». Mais, plutôt que de mettre en œuvre la règle établissant que les OGM à une seule modification doivent faire l’objet d’une autorisation dédiée, les États membres discutent d’en affranchir le colza Ms11. La Commission européenne explique justement que le pétitionnaire lui a demandé de bien vouloir mettre en attente la demande concernant le colza Ms11, en attendant que les experts européens aient terminé leur analyse des risques liés à l’OGM empilé Ms11*Rf3. Une requête à laquelle la Commission déclare alors avoir accédé.
Trois semaines plus tard, le même comité [7] tente de généraliser à tous les OGM ce cas particulier. Un État membre explique « brièvement (…) sa proposition concernant l’approche de l’évaluation des risques qui devrait être adoptée dans le futur concernant des produits similaires ». Le contenu de la proposition n’est pas développé mais le compte-rendu de la réunion du 19 avril 2021 [8] permet de comprendre qu’il s’agit d’exonérer les OGM à une seule modification génétique d’une demande d’autorisation dédiée s’ils ne sont pas voués à être commercialisés en tant que tels.
… pour une règle généralisable !
À cette réunion, un État membre explique en effet que « dans le cas de produits non destinés à la commercialisation mais voués uniquement à être utilisés dans un empilement, l’évaluation des risques de l’OGM à une modification et celle de l’OGM empilé devraient être gérées dans le cadre d’une seule demande d’autorisation ». Le compte-rendu indique que « certains États membres » partagent cette vision. Mais un État suggère que « les comités nationaux d’évaluation des risques et l’AESA puissent discuter de l’évaluation des risques de ce type de produits avant toute autre discussion » au niveau des instances politiques. La Commission européenne a rappelé aux États l’obligation légale d’évaluation des risques pour les modifications seules, mais, magnanime, elle a ajouté « reconnaître malgré tout que d’autres discussions seraient utiles sur la manière de conduire une évaluation dans de tels cas »…
Ces discussions vont donc continuer entre États membres et Commission européenne mais on peut d’ores et déjà supposer qu’elles seront plus politiques que scientifiques. Car un paradoxe important émerge de l’historique de ce dossier tel que rappelé dans cet article. En 2013, la décision d’étendre une autorisation pour un OGM empilé à toutes les sous-combinaisons était argumenté par l’apparition de ces sous-combinaisons lors de la mise en culture d’OGM empilé, le règlement 503/2013 soulignant même que leur commercialisation est donc « inévitable ». En 2021, cette argument est oublié lorsqu’il s’agit d’envisager cette fois d’inclure les OGM à une seule modification dans l’autorisation de l’OGM empilé. Peu importe qu’un tel OGM à une modification soit commercialisé de manière « inévitable », l’important est que le pétitionnaire n’ait pas « l’intention de le commercialiser »…
[1] ,
, « OGM : un encadrement en mode allégé », Inf’OGM, 11 octobre 2018
[2] ,
, « Autorisations d’OGM : des allègements passés inaperçus », Inf’OGM, 17 octobre 2018
[3] ,
, « OGM – Quelle légalité de l’autorisation des sous-combinaisons ? », Inf’OGM, 22 octobre 2018
[4] Considérant 18 du règlement 503/2013.
[5] ,
, « Autorisations d’OGM : des allègements passés inaperçus », Inf’OGM, 17 octobre 2018