Crispr / Cas9 : des nouveaux ciseaux à ADN
Certaines techniques de biotechnologie utilisent des protéines capables de couper l’ADN comme des ciseaux : nucléases à doigt de zinc, méganucléases ou encore TALENs [1]. Cette famille de protéines vient d’accueillir un nouvel arrivant, au nom barbare de Crispr/Cas9. L’objectif est le même : couper le génome à un endroit pour y induire une mutation ou y insérer un gène. La différence entre ces techniques se situe au niveau de l’outil utilisé : une protéine, plusieurs protéines, une protéine en complexe avec un ARN… Chacun de ces outils a un niveau différent de précision pour couper le génome et une « facilité » d’utilisation différente.
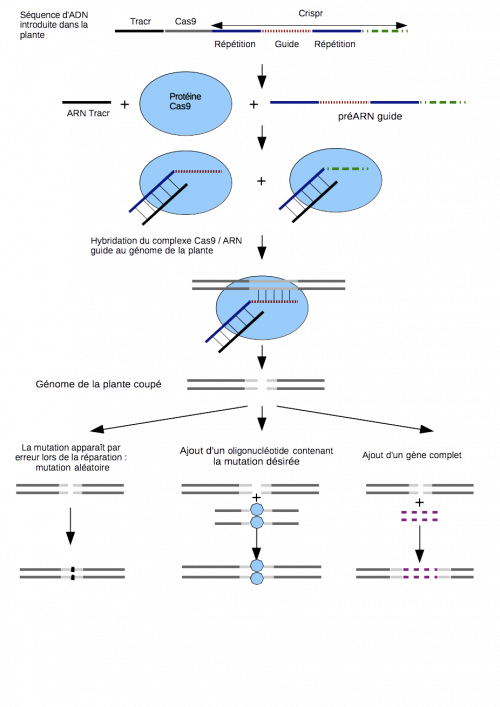
Le nom Crispr/Cas9 s’applique aussi bien à la technique qu’à la construction génétique introduite dans les cellules végétales. Dans le détail, cette construction génétique se compose de trois éléments : Cas9, Crispr et Tracr (cf. schéma).
La séquence Tracr code un ARN qui s’hybridera avec l’ARN guide dont nous allons parler. La séquence Cas9 code la protéine de même nom, protéine qui appartient à la famille des nucléases dont l’activité est de couper le génome comme un ciseau. Les séquences génétiques Crispr sont des groupes de séquences répétées à intervalles réguliers (Clustered Regularly Interspaced Short Palindromic Repeats, Crispr). Ces séquences sont présentes dans le génome de bactéries et de microorganismes unicellulaires très anciens appelés archées. Leur rôle n’est cependant pas encore complètement compris. Il pourrait être de participer à la réparation du génome mais aussi être un mécanisme de défense des bactéries et archées (ou archéobactéries) contre des phages (virus infectant les bactéries) [2]. Comme le montre le schéma, il est en tout cas montré que le complexe Crispr/Cas9 est utilisable pour modifier le génome.

Comment cela fonctionne ?
Les constructions génétiques Crispr/Cas9 sont préférentiellement apportées dans une cellule végétale en utilisant la bactérie Agrobacterium tumefaciens pour infecter les cellules végétales et y transférer la construction génétique souhaitée. Cette construction génétique utilisera ensuite la machinerie cellulaire de production de protéines pour remplir son rôle. Plusieurs séquences vont remplir un rôle précis : la séquence d’ADN Cas9 permet à la cellule de produire la protéine Cas9 – la séquence Tracr permet à la cellule de produire un petit ARN du même nom – la séquence Crispr permet à la cellule de produire les ARN guides qui, en s’hybridant à l’ARN Tracr et s’accrochant à la protéine Cas9, permettront de guider la protéine jusqu’au lieu du génome végétal à couper.
Une fois accrochée au génome végétal, la protéine Cas9 remplira sa fonction de nucléase en coupant l’ADN. A partir de là, soit la cellule répare elle-même cette coupure avec un certain taux d’erreur, soit une séquence d’ADN tierce a également pu être introduite afin de servir de matrice pour réparer l’ADN et induire ainsi une mutation spécifique, soit un (trans/cis)gène a également été introduit et sera alors inséré au lieu de coupure.
Quels « avantages » par rapport aux autres systèmes de coupure du génome ?
Le premier avantage concret que représente cette technique pour les techniciens de laboratoire est de pouvoir être déclinée plus facilement que les méganucléases, Talen ou autre nucléases à doigt de zinc. Car avec Crispr/Cas9, il « suffit » aux techniciens de changer la seule séquence guide pour que cet outil soit utilisé pour différents lieux de coupure. Dans le cas des nucléases à doigt de zinc par exemple, il est nécessaire de reconfigurer l’ensemble de l’outil pour le faire changer de cible. Par ailleurs, le complexe Crispr/Cas9 coupe l’ADN plus précisément que les protéines Talen dont le niveau de précision était pourtant – et est toujours – un des arguments « de vente ».
Imprécision mais brevets
Plus précise, cette technique n’est cependant pas non plus fiable à 100 %. Ainsi, d’autres lieux du génome peuvent être coupés (si l’ARN servant de guide les « reconnaît » et s’y fixe). Ce qui induit donc la possibilité d’apparition de mutations en d’autres endroits du génome, avec toute la difficulté que représente l’ignorance du lieu pour pouvoir détecter et se débarrasser de ces mutations.
Surtout, cette technique fait d’ores et déjà l’objet de dépôt de brevets, impliquant donc la présence de droits de propriété industrielle suite à son utilisation. Ainsi, la revue Nature avait recensé en avril 2014 dix demandes de brevets aux États-Unis, en Chine, en Russie et en Nouvelle-Zélande [3]. Il s’agit de plusieurs brevets car, à l’instar des autres techniques de biotechnologie, le principe de la technique n’est pas le seul objet du brevet. Ces derniers sont ainsi déposés pour différentes natures de protéines Cas et différentes séquences ciblées dans le génome…
Quelles utilisations ?
La technique Crispr/Cas9 s’utilise tant sur les organismes animaux (dont l’homme dans le cas de thérapie génique), que végétaux ou sur des microorganismes. Elle est utilisée pour induire des mutations, insérer des trans/cisgènes, enlever des gènes présents dans l’organisme ou bien inhiber leur expression… Mais cette technique en est encore à ses débuts et la plupart des utilisations sont encore au stade de projet. Certaines structures offrent néanmoins déjà des kits Crispr/Cas9 prêts à l’emploi comme les entreprises étasuniennes Origene, Caribou Bioscience, ERS Genomics… Et la technique elle-même se diffuse également par le biais d’accords de licence [4].
[1] , « Les citoyens face à l’explosion des techniques de biotechnologies », Inf’OGM, 24 janvier 2014
[2] Les séquences Crispr donneraient des ARN qui sont ensuite découpés en petits ARN. Les séquences guides seraient capables de se lier à des séquences virales par exemple. En s’hybridant à ces séquences virales, ces ARN provoqueraient leur dégradation ou les empêcheraient de jouer leur rôle dans le cycle viral. Ce dernier serait alors inhibé.
[3] Cf. les brevets WO2013188037A2, US20130288251A1, NZ597299A, RU2011122776A et encore CN102264895A.